

En este articulo vamos a tratar de forma resumida el papel de los ácidos grasos de cadena corta (AGCC o SCAF) y su posible papel en la modulación de la tolerancia intestinal, así como su mediación en las alergias alimentarias según las últimas investigaciones en materia 1.
Los AGCC (acetato, propionato, butirato y pentanoato) son uno de los miles de metabolitos secundarios producto de la fermentación de carbohidratos complejos, como la fibra dietética; por parte de la microbiota intestinal 2.
Estos compuestos derivados del metabolismo de las bacterias intestinales tienen múltiples funciones sobre diversos procesos fisiológicos en el huésped e incluso participan en su regulación, ofreciendo así ciertos beneficios sobre la salud intestinal 3. Entre otros mucho efectos son capaces de incidir en los procesos de inflamación y procesos autoinmunes de forma local en el intestino 4,5, modulando de esta manera el efecto y consecuencias de estos procesos sobre el organismo.
Debido a que la enfermedad celiaca es un patología mediada por la activación del sistema inmune y que cursa con un proceso de inflamación del epitelio intestinal 6, es posible considerar que estos metabolitos tengan efectos terapéuticos beneficiosos, no solo sobre esta enfermedad; si no sobre la distinta variedad de trastornos gastrointestinales incluyendo las enfermedades inflamatorias intestinales (EII) y alergias alimentarias.
Como ya hemos comentado, los AGCC participan en diversos procesos fisiológicos en el huésped, entre ellos se sabe que son capaces de modular la proliferación y diferenciación del epitelio intestinal, así como del sistema inmunológico de este por distintas vías de acción:
Por un lado, los AGCC funcionan como moléculas de señalización por medio de los receptores GPR expresados por las células no solo del epitelio intestinal si no también del sistema inmune. Una vez producida esta unión se activa una cascada de señalización con diferentes consecuencias sobre los distintos niveles del tejido intestinal 7. Una de ellas es que se promueve la proliferación de las células o linfocitos T reguladores (células Tregs), los cuales tienen la función de controlar la respuesta inmune frente a partículas extrañas (los antígenos), restaurar la homeostasis y favorecer la tolerancia hacia autoantígenos 8. Recientemente se ha demostrado que los linfocitos T de intestino delgado tienen la capacidad de reconocer los antígenos de la dieta y limitan las reacciones adversas regulando una respuesta inmune de tipo supresora 9.
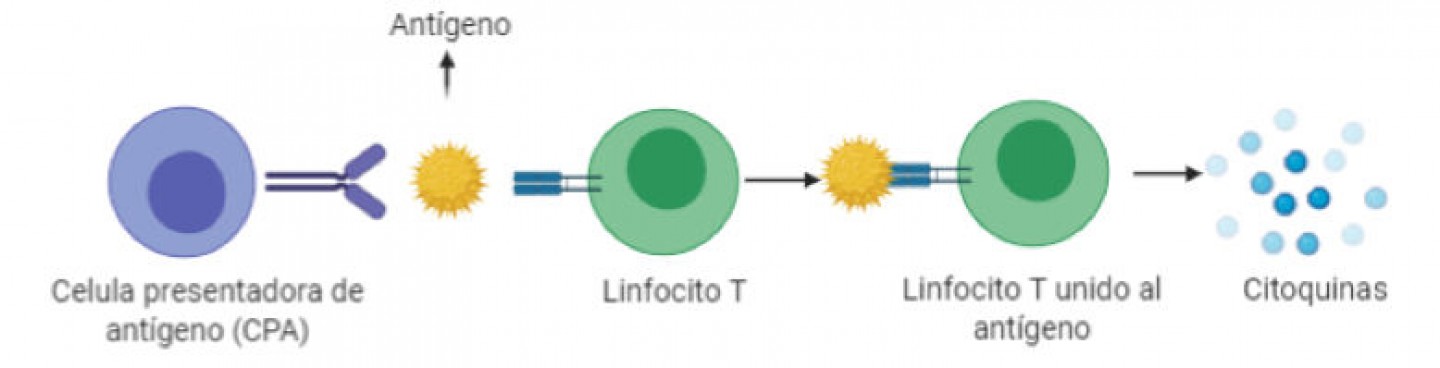
Las citoquinas liberadas por los linfocitos T serán las encargadas de mediar con los antígenos dietarios que causan las reacciones de intolerancia.
Además, recientemente se ha descubierto que el ácido retinoico , metabolito derivado de la Vit A; actúa de forma sinérgica con los AGCC para controlar la respuesta inmune frete a antígenos dietarios mediante la reducción de citoquinas proinflamatorias y la inducción de linfocitos T 10,11.
De esta manera, los AGCC estarían favoreciendo ciertos efectos tolerogénicos a nivel intestinal 12 y suponiendo también beneficios importantes para la tolerancia intestinal y las EII 13 .
Por otro lado, el butirato y el propionato en concreto son capaces de regular la modulación de genes relacionados con la proliferación y diferenciación celular, con la integridad del epitelio y de la barrera por medio de cambios epigenéticos 14,15 , influyendo así sobre la tolerancia a proteínas dietéticas 16 y previniendo de esta manera la aparición de canceres sobre todo colorrectales 17.
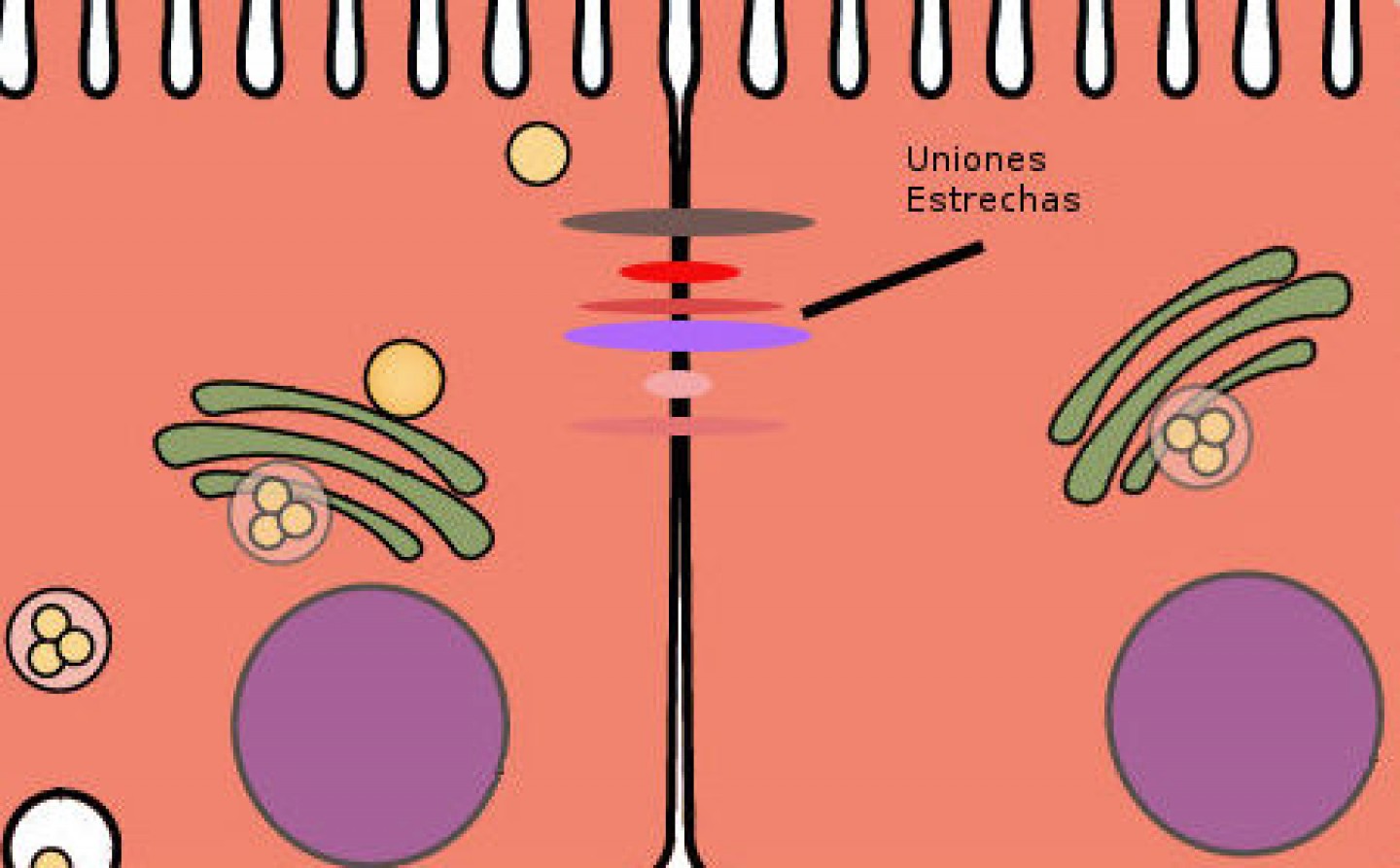
Los AGCC son capaces de favorecer el mantenimiento de la homeostasis y la barrera intestinal por medio de la activación del factor inducible por hipoxia (HIF), un factor de transcripción crucial para la regulación de los genes implicados en la integridad intestinal) 18. De esta manera promueven las uniones estrechas entre los enterocitos disminuyendo así la permeabilidad intestinal y favorecen la producción mucina 19,20 y IL-18, cruciales para la tolerancia bacteriana y el control de la homeostasis intestinal 21.
Además, se sabe que la forma dominante en la que se presenta la alergia alimentaria es la mediada las IgE 22. Estudios recientes sugieren que os AGCC actuarían de forma sinérgica con componentes de la dieta como el ácido retinoico y proteínas dietarías para regular epigeneticamente diversas células del sistema inmune mediando de esta manera sobre la reacción alérgica 23,24.
Como conclusión de toda la evidencia recogida, destacamos que estas moléculas producidas de manera natural por la microbiota podrían ser fuente de numerosos beneficios para la salud del huésped y ejercerían efectos positivos sobre el control del sistema inmune y la reacción inflamatoria que tanto afecta a patologías como la celiaquía, colitis, Crohn, etc. Es por ello por lo que creemos que esta línea de investigación podría arrojar resultados prometedores para el tratamiento terapéutico de esas patologías y abriría una oportunidad al desarrollo de nuevos productos destinados a estos enfoques terapéuticos en materia de tolerancia y alergias alimentarias.

Bibliografía:
1. Luu, M., Monning, H. & Visekruna, A. Exploring the Molecular Mechanisms Underlying the Protective Effects of Microbial SCFAs on Intestinal Tolerance and Food Allergy. Front. Immunol. 11, 1225 (2020).
2. Cummings, J. H., Pomare, E. W., Branch, H. W. J., Naylor, C. P. E. & MacFarlane, G. T. Short chain fatty acids in human large intestine, portal, hepatic and venous blood. Gut 28, 1221–1227 (1987).
3. Blumberg, R. & Powrie, F. Microbiota, disease, and back to health: A metastable journey. Science Translational Medicine vol. 4 (2012).
4. Kim, C. H., Park, J. & Kim, M. Gut Microbiota-Derived Short-Chain Fatty Acids, T Cells, and Inflammation. Immune Netw. 14, 277 (2014).
5. Luu, M. & Visekruna, A. Short-chain fatty acids: Bacterial messengers modulating the immunometabolism of T cells. European Journal of Immunology vol. 49 842–848 (2019).
6. Ludvigsson, J. F. et al. The Oslo definitions for coeliac disease and related terms. Gut 62, 43–52 (2013).
7. Sivaprakasam, S., Prasad, P. D. & Singh, N. Benefits of short-chain fatty acids and their receptors in inflammation and carcinogenesis. Pharmacology and Therapeutics vol. 164 144–151 (2016).
8. Peterson, R. A. Regulatory T-Cells: Diverse Phenotypes Integral to Immune Homeostasis and Suppression. Toxicol. Pathol. 40, 186–204 (2012).
9. Kim, K. S. et al. Dietary antigens limit mucosal immunity by inducing regulatory T cells in the small intestine. Science (80-. ). 351, 858–863 (2016).
10. Tan, J. et al. Dietary Fiber and Bacterial SCFA Enhance Oral Tolerance and Protect against Food Allergy through Diverse Cellular Pathways. Cell Rep. 15, 2809–2824 (2016).
11. Yap, Y. A. & Mariño, E. An insight into the intestinal web of mucosal immunity, microbiota, and diet in inflammation. Frontiers in Immunology vol. 9 2617 (2018).
12. Singh, N. et al. Activation of Gpr109a, receptor for niacin and the commensal metabolite butyrate, suppresses colonic inflammation and carcinogenesis. Immunity 40, 128–139 (2014).
13. Smith, P. M. et al. The microbial metabolites, short-chain fatty acids, regulate colonic T reg cell homeostasis. Science (80-. ). 341, 569–573 (2013).
14. Park, J. et al. Short-chain fatty acids induce both effector and regulatory T cells by suppression of histone deacetylases and regulation of the mTOR-S6K pathway. Mucosal Immunol. 8, 80–93 (2015).
15. Schilderink, R. et al. The SCFA butyrate stimulates the epithelial production of retinoic acid via inhibition of epithelial HDAC. Am. J. Physiol. Liver Physiol. 310, G1138–G1146 (2016).
16. Goverse, G. et al. Diet-Derived Short Chain Fatty Acids Stimulate Intestinal Epithelial Cells To Induce Mucosal Tolerogenic Dendritic Cells. J. Immunol. 198, 2172–2181 (2017).
17. Zeng, H., Umar, S., Rust, B., Lazarova, D. & Bordonaro, M. Secondary bile acids and short chain fatty acids in the colon: A focus on colonic microbiome, cell proliferation, inflammation, and cancer. International Journal of Molecular Sciences vol. 20 (2019).
18. Kelly, C. J. et al. Crosstalk between microbiota-derived short-chain fatty acids and intestinal epithelial HIF augments tissue barrier function. Cell Host Microbe 17, 662–671 (2015).
19. Feng, Y., Wang, Y., Wang, P., Huang, Y. & Wang, F. Short-Chain Fatty Acids Manifest Stimulative and Protective Effects on Intestinal Barrier Function Through the Inhibition of NLRP3 Inflammasome and Autophagy. Cell. Physiol. Biochem. 49, 190–205 (2018).
20. Burger-van Paassen, N. et al. The regulation of intestinal mucin MUC2 expression by short-chain fatty acids: Implications for epithelial protection. Biochem. J. 420, 211–219 (2009).
21. Kalina, U. et al. Enhanced production of IL-18 in butyrate-treated intestinal epithelium by stimulation of the proximal promoter region. Eur. J. Immunol. 32, 2635–2643 (2002).
22. Tordesillas, L., Berin, M. C. & Sampson, H. A. Immunology of Food Allergy. Immunity vol. 47 32–50 (2017).
23. Hara, S. et al. Dietary Antigens Induce Germinal Center Responses in Peyer’s Patches and Antigen-Specific IgA Production. Front. Immunol. 10, 2432 (2019).
24. Visekruna, A. et al. Intestinal development and homeostasis require activation and apoptosis of diet-reactive T cells. J. Clin. Invest. 129, 1972–1983 (2019).